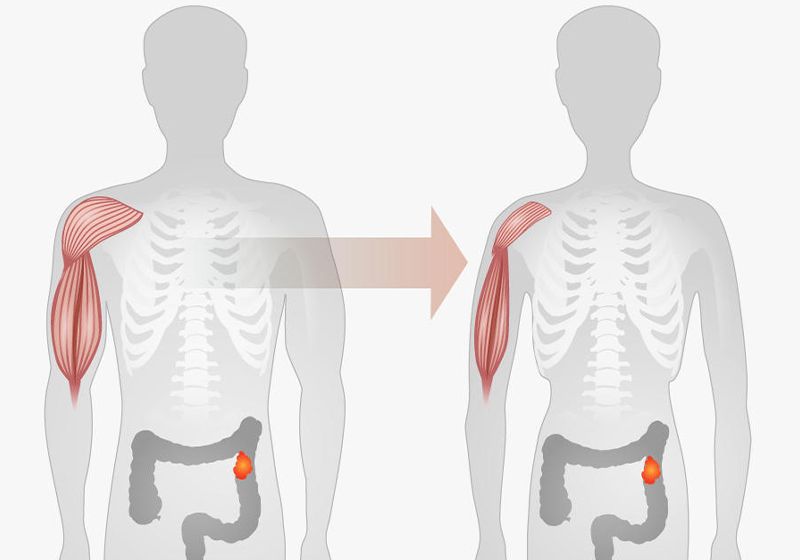
docaquexia ancestralo síndrome de emaciación, es una condición catastrófica que causa una pérdida dramática e involuntaria de masa muscular, grasa y peso, junto con fatiga extrema, anorexia y anemia en pacientes con cáncer.1 Este estrés severo reduce la capacidad del cuerpo para responder a los tratamientos, empeorando el pronóstico y acelerando drásticamente la muerte.
“La mayoría de las veces, si tienes dos pacientes que tienen exactamente la misma etapa de la enfermedad, patología de la enfermedad, pero uno de esos cánceres descubrió cómo promover la emaciación en el cuerpo, [that person] vivirá la mitad que la otra persona”, dijo Puneeth Iyengaroncólogo radioterapeuta del Centro Oncológico Memorial Sloan Kettering.
La caquexia afecta aproximadamente entre el 50 y el 80 por ciento de los pacientes con cáncer y es la principal causa de muerte en el 30 por ciento de los pacientes. Sin embargo, faltan remedios sólidos para esta afección. “No sabemos lo suficiente sobre [cancer cachexia] biología. Es un problema muy complejo”, dijo Iyengar.
En un estudio reciente publicado en Comunicaciones de la naturaleza, un equipo de investigadores del Laboratorio Cold Spring Harbor (CSHL) arrojar luz sobre los mecanismos neuronales que impulsan esta afección.2 Los hallazgos revelaron nuevos objetivos que podrían informar el desarrollo de terapias que mejoren la calidad de vida de los pacientes que padecen esta afección.
Las células cancerosas modulan el tejido circundante y los órganos distantes a través de las moléculas que secretan. Uno de esos mensajeros multifuncionales, la interleucina-6 (IL-6), es un factor clave de la caquexia por cáncer. Muchos pacientes con esta afección exhibieron niveles elevados de citocina en sangre. Los estudios en roedores sugieren que el exceso de IL-6 puede afectar reacciones fisiológicas controladas por el cerebro, como la necesidad de comer o la fiebre. Sin embargo, se desconocía si la IL-6 activa los receptores en el cerebro para desencadenar síntomas caquécticos.
El estudio comenzó con una colaboración improvisada entre biólogos oncológicos Tobías Janowitz y neurocientífico boliambos en CSHL. Li recordó que, a pesar de múltiples conversaciones en las que Janowitz sugirió colaborar para explorar el papel del cerebro en la caquexia, no estaba seguro de cómo podría contribuir; se mostró escéptico acerca de cómo un modelo de roedor podría ayudar a decodificar un problema fisiológico tan complejo que implica un síndrome de síntomas. Sin embargo, después de observar que los ratones con caquexia presentaban niveles elevados de IL-6 en la sangre, seguidos de síntomas clásicos de caquexia como anorexia y una pérdida de peso espectacular, Li se convenció de su potencial.
Lo primero que probaron Li y el equipo fue dónde viaja y actúa la IL-6 en los ratones modelo de caquexia. Inyectaron a ratones sanos y caquécticos IL-6 marcada con un marcador molecular y examinaron sus cerebros tres horas después. Para su sorpresa, en todo el cerebro de ratones sanos y caquécticos, encontraron IL-6 solo en una región: el área postrema (AP), una estructura del tronco del encéfalo. Utilizando el marcador de actividad neuronal Fos, el equipo observó que la inyección de IL-6 aumentaba la actividad de las neuronas y células AP en las regiones del cerebro conectadas a la AP, incluidas áreas del hipotálamo y la amígdala. Anteriormente se demostró que un subconjunto de células AP activadas causaba náuseas y caquexia por cáncer en ratones.3
Cuando el equipo de investigación inyectó IL-6 en el torrente sanguíneo (rosa) de ratones sanos (fila superior) y caquécticos (fila inferior), la detectaron solo en una región del cerebro, la AP.
Para determinar si el cáncer por sí solo podría aumentar la actividad de las neuronas AP, el equipo recurrió a un modelo de ratón con cáncer de colon. Después de la formación del tumor, los niveles de IL-6 aumentaron en la AP. Unos días más tarde, el equipo de investigación observó un aumento en el número de neuronas activas en la AP seguido de una mayor actividad en las regiones cerebrales conectadas. Sólo después de que ocurrieron estos cambios se manifestó la caquexia.
Una vez que la condición se presenta, rápidamente puede causar estragos; Li y su equipo observaron que algunos ratones perdieron el 10 por ciento de su peso corporal en un solo día. Para aliviar estos síntomas, los investigadores colocaron una bomba en miniatura en las cabezas de los ratones y administraron anticuerpos contra la IL-6 al líquido cefalorraquídeo. El tratamiento redujo con éxito los síntomas de la caquexia tanto cuando se administró en una etapa tardía de la enfermedad como antes de que se desarrollara el tumor. Los ratones que recibieron la infusión comieron más comida, bebieron más agua, perdieron menos peso y vivieron más que los ratones no tratados. El anticuerpo también redujo la hiperactividad neuronal en la AP y sus regiones conectadas.
“Lo que más me sorprendió fue que nuestra manipulación en una pequeña área del cerebro, sin tantas neuronas allí, en una condición muy grave, puede hacer que el animal sobreviva mucho más tiempo”, dijo Li. Para demostrar causalmente que las neuronas AP impulsan la caquexia, el equipo utilizó un Sistema CRISPR/dCas9 para amortiguar los niveles de Il6rael gen del receptor de IL-6, en estas células y dos semanas después inoculó a los ratones con células tumorales. Estos ratones no sólo exhibieron menos actividad neuronal en el AP, sino que también mostraron menos síntomas caquécticos en relación con los ratones con niveles normales del gen. Estos resultados confirmaron que los niveles altos de IL-6 en el cáncer pueden hacer que la red AP se hiperimpulse, activando una cascada de síntomas que resultan en el desarrollo del síndrome de emaciación. El equipo observó los mismos resultados en modelos murinos de cáncer ductal de páncreas y carcinoma de pulmón de Lewis.
A continuación, Li quiere determinar si los pacientes humanos presentan cambios similares inducidos por la caquexia en la actividad AP. También está interesado en extraer datos para desarrollar terapias mejores y más específicas para tratar la afección.
“La gente siente que tal vez sea casi imposible curar la caquexia. Pero si podemos minimizar los síntomas de caquexia, eso le dará al paciente la oportunidad de someterse a la terapia estándar para el cáncer y tener más posibilidades de sobrevivir”, afirmó Li.