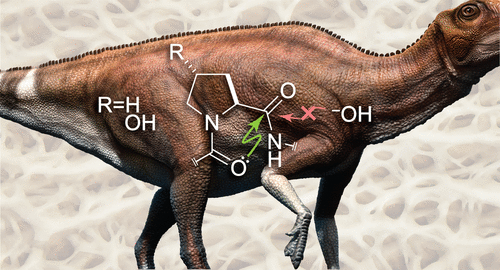
El colágeno es la proteína más abundante en los animales y también una de las más duraderas. En las últimas décadas, los paleontólogos lo han encontrado en fósiles de dinosaurios de decenas de millones de años de antigüedad.
Su persistencia es desconcertante, porque la proteína contiene enlaces químicos que, sobre el papel, deberían durar sólo 500 años. ¿Por qué, entonces, dura tanto? Los químicos dan respuesta a ese misterio en un artículo Centro de Ciencias de la ACS informe.
La fuerza del colágeno
La respuesta comienza con la estructura del colágeno. El colágeno está formado por tres cadenas de proteínas que, básicamente, se entrelazan para formar una sustancia mucho más fuerte que cada cadena.
“Las hebras de colágeno forman una triple hélice”, dice Ron Rainesquímico del Instituto Tecnológico de Massachusetts y autor del artículo. “Esa triple hélice es una estructura notable que ha servido como andamiaje para los cuerpos de los animales durante (al menos) 200 millones de años. Me pregunto si la evolución de la triple hélice de colágeno permitió que la vida animal surgiera en la Tierra hace aproximadamente mil millones de años”.
Sin embargo, incluso la cuerda más resistente se desgasta, se deshilacha y, con el tiempo, acaba rompiéndose. Entonces, ¿por qué no funciona el colágeno?
Leer más: El análisis del hueso ayuda a explicar por qué es tan fuerte
Cómo el colágeno resiste el agua
Ese es el misterio que se esconde tras la longevidad del colágeno. Los aminoácidos, que forman cada hebra de la cuerda de colágeno, normalmente se descomponen cuando se exponen al agua, al igual que una cuerda normal se desgasta con la lluvia. Por alguna razón, los enlaces peptídicos (esencialmente el pegamento químico que mantiene unidas las hebras) que conectan los aminoácidos en el colágeno no se descomponen cuando se mojan.
Para investigar por qué no, los químicos diseñaron y sintetizaron pequeñas moléculas que les permitieron probar cómo reaccionaban a los enlaces peptídicos vecinos en el colágeno.
“En esencia, podríamos ‘activar’ o ‘desactivar’ esa interacción y luego observar los resultados”, dice Raines. Estaban especialmente interesados en observar la hidrólisis, el proceso por el cual el agua descompone las sustancias químicas.
“Descubrimos que activar la interacción impedía la hidrólisis”, afirma Raines.
Compartición de electrones y principio de exclusión de Pauli
El cómo es un poco esotérico, ya que implica un efecto mecánico cuántico llamado “principio de exclusión de Pauli”.
El principio Establece que un orbital en una molécula puede estar ocupado por hasta dos electrones, no más. Debido a que los componentes del colágeno comparten electrones en toda su estructura, esencialmente no hay espacio para que los electrones en una molécula de agua alteren los enlaces.
“El colágeno es único porque permite este intercambio de electrones en toda su estructura”, afirma Raines. “Ninguna otra proteína está tan protegida de la hidrólisis”.
Ahora que sabemos por qué nuestros huesos y cartílagos, ricos en colágeno, son tan resistentes, ¿qué pueden hacer los científicos con esa información? Los investigadores ya han demostrado cómo diseñar enlaces similares para que sean vulnerables al agua, incluso en los cubiertos biodegradables.
“¡Seguro que también se pueden hacer aplicaciones similares!”, afirma Raines.
Leer más: Primera observación de un cristal cuántico de Pauli
Artículo Fuentes
Nuestros escritores en Discovermagazine.com Utilizamos estudios revisados por pares y fuentes de alta calidad para nuestros artículos, y nuestros editores revisan la precisión científica y los estándares editoriales. Revise las fuentes utilizadas a continuación para este artículo:
Antes de unirse a Discover Magazine, Paul trabajó durante más de 20 años como periodista científico, especializándose en políticas de ciencias biológicas en Estados Unidos y en cuestiones relacionadas con la carrera científica a nivel mundial. Comenzó su carrera en periódicos, pero luego se pasó a revistas científicas. Su trabajo ha aparecido en publicaciones como Science News, Science, Nature y Scientific American.