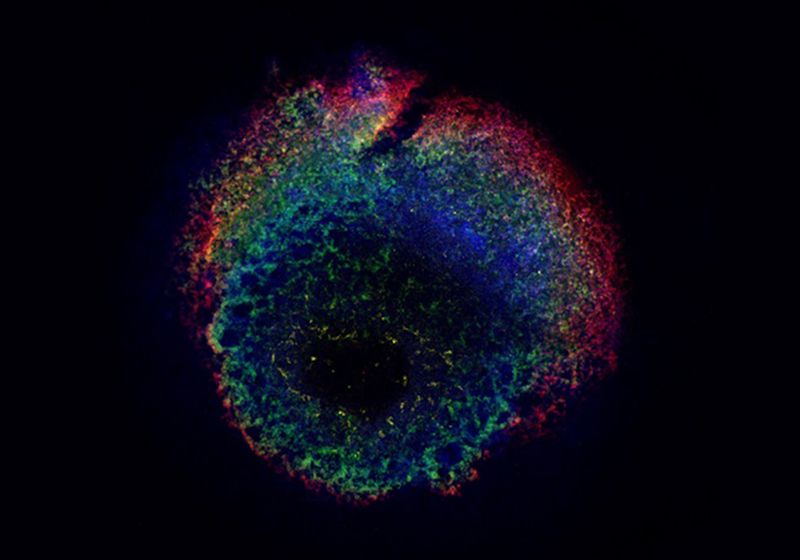
GRAMOExtraer sangre de una piedra es imposible, pero cultivar sangre a partir de minicorazones 3D ya es una realidad. Un equipo de investigación dirigido por Robert Zweigerdtbiólogo del desarrollo de la Facultad de Medicina de Hannover, utilizó anteriormente células madre pluripotentes humanas para producir organoides formadores de corazón (HFO) en un plato.1 Estas mini construcciones de corazón primordial muestran las múltiples capas de tejido que existen en el corazón humano en desarrollo. También contienen la capacidad latente de producir células sanguíneas. En un estudio reciente publicado en Biología celular de la naturalezaZweigerdt y su equipo modificaron su modelo HFO para crear HFO generadores de sangre (BG), que recapitulan aspectos clave del desarrollo de las células sanguíneas embrionarias.2
Mucho antes de que la médula ósea humana asuma la tarea de producir sangre, se producen ondas discretas de producción de células sanguíneas en el embrión en desarrollo. Miriana Dardanoinvestigador postdoctoral en el laboratorio de Zweigerdt y coautor del estudio, modificó el modelo HFO original utilizando cócteles de citoquinas y factores de crecimiento que alentaron a estos organoides a producir células sanguíneas, incluidos eritrocitos, monocitos y macrófagos. El resultado fue un organoide de múltiples tejidos formado por tejidos cardíacos, endoteliales y hematopoyéticos.
“Fue muy agradable ver que, tras modificar el protocolo, es posible modelar la hematopoyesis en un sistema que ya está recapitulando aspectos del desarrollo del corazón. Esto se debe a que los tejidos hematopoyético, endotelial y cardíaco se derivan del mismo tejido embrionario”, dijo Dardano. “Desde el punto de vista del desarrollo, tiene sentido. Tenemos todos esos tejidos desarrollándose simultáneamente y [follow] un patrón específico que recapitula la morfología de la región intraembrionaria donde se desarrolla el tejido cardíaco y surge la hematopoyesis”.
La embriogénesis depende de un programa reproducible y finamente orquestado de formación de patrones que crea las estructuras de múltiples tejidos que eventualmente se convierten en órganos. El corazón humano no es una excepción y, al imitar su diseño de tejido altamente conservado, el equipo de Zweigerdt creó nuevas oportunidades para modelar enfermedades. “Con estos organoides ahora podemos estudiar in vitro los mecanismos del desarrollo humano. Lo realmente emocionante es [the potential] para un modelado in vitro más complejo de enfermedades congénitas [heart] enfermedades”, dijo Zweigerdt. “La consecuencia de, digamos, una desactivación genética o una modulación química que modifica el desarrollo se expresará en la formación de este patrón, que es algo que se puede monitorear con relativa facilidad mediante microscopía”. Por ejemplo, el modelo BG-HFO se puede utilizar para comprender mejor cómo la exposición intraútero al tabaco o ciertas drogas causa defectos cardíacos congénitos. El modelo también tiene potencial para aplicaciones de detección de fármacos y medicina regenerativa.
Robert Zweigerdt (izquierda) dirige un grupo de investigación en los Laboratorios de Investigación Leibniz de Biotecnología y Órganos Artificiales (LEBAO) de la Facultad de Medicina de Hannover. Junto con los miembros del equipo Miriana Dardano (centro) y Lika Drakhlis (derecha), Zweigerdt supera los límites de la ciencia con un enfoque de cultivo celular de vanguardia para crear organoides multitejidos que generan sangre y forman calor.
Karin Káiser
Lika Drakhlisinvestigador postdoctoral en el laboratorio de Zweigerdt y coautor del estudio, fue el primero en crear el modelo HFO original. “Es muy fascinante hacer biología del desarrollo en una placa, ver qué sucede en el embrión, qué sucede con las células madre”, dijo Drakhlis. En el caso del modelo BG-HFO, la clave fue descubrir cómo dirigir las células madre con la combinación justa de señales químicas para impulsarlas por una vía de desarrollo que imite la embriogénesis del corazón. El hecho de que recapitularan el desarrollo de la sangre embrionaria fue extraordinario. “Me alegré mucho y me sorprendió ver que el modelo es más potente de lo que jamás podría imaginar”, dijo Drakhlis.
Sridhar Raoun científico clínico e investigador del Versiti Blood Research Institute que no participó en este estudio, considera este trabajo como un avance importante. “Me sorprendió que con algunos ajustes sutiles pudieran obtener unidades formadoras de sangre a partir de los organoides formadores de corazón”, dijo Rao. “Durante el desarrollo embrionario normal de los mamíferos placentarios, el sistema sanguíneo y el sistema cardiovascular se desarrollan al mismo tiempo, pero la influencia de los dos [on each other] Ha sido extremadamente difícil de estudiar. Este trabajo es un avance importante en el campo porque permite estudiar ambos de una manera más mecanicista en un plato”.
Zweigerdt espera explorar todo el potencial del modelo BG-HFO. “La madurez de estos tejidos es limitada, algo en lo que estamos trabajando para ver si se puede desarrollar más hacia [greater] maduración”, dijo Zweigerdt. Por ahora, los corazones primordiales brindan una visión fascinante de cómo se codesarrollan las células cardíacas, endoteliales y hematopoyéticas multipotentes humanas, poniendo la carne y la sangre del desarrollo embrionario al alcance de los científicos.