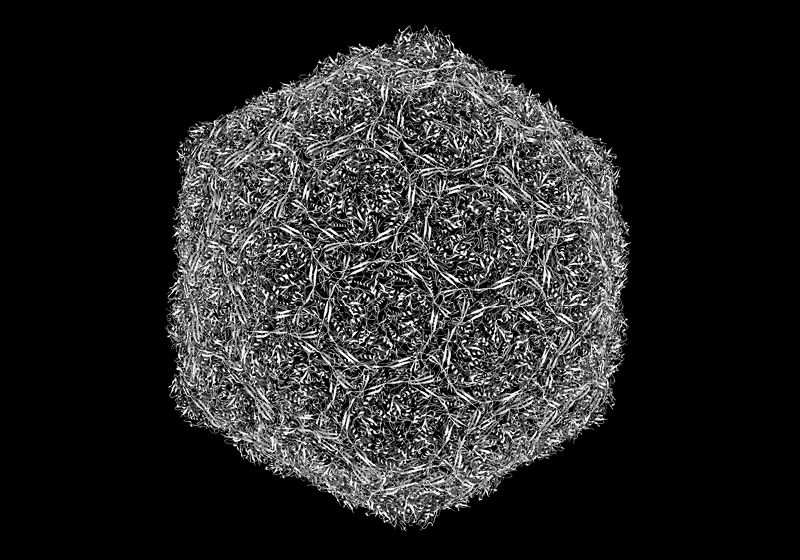
A El virus puede ser microscópico, pero contiene miles de bases de ácido nucleico estratégicamente empaquetadas en una cubierta proteica. Saber cómo el virus organiza estos vastos almacenes de información en un espacio compacto es la clave para comprender la estructura viral y diseñar mejores defensas contra los virus patógenos.
Escudriñar la cubierta de proteína viral, o cápside, es un desafío. Las técnicas típicas de discernimiento de estructuras, como la microscopía crioelectrónica, no pueden capturar las diferentes configuraciones del material genético en cada virus. En 2010, Alekséi Aksimétiev, biofísico de la Universidad de Illinois Urbana-Champaign, tuvo una idea para simular computacionalmente la estructura de un virus. Sin embargo, los métodos computacionales simplemente no eran lo suficientemente sofisticados en ese momento.
“Siempre estuvo en el fondo de nuestras mentes, y luego logramos un gran avance en términos de metodología”, dijo Aksimentiev.
Ahora, 14 años después, en un estudio publicado en Naturalezasu equipo informó que utiliza un nuevo enfoque computacional para simular los átomos individuales de un virus que está repleto de ácidos nucleicos.1 Utilizaron este método para estudiar el bacteriófago HK97 y propusieron la primera estructura del virus.
Hace unos años, el equipo de Aksimentiev desarrolló un método para mapear configuraciones complejas de ADN simulándolas computacionalmente en múltiples resoluciones.2 Comienzan con una resolución aproximada, como una imagen borrosa, y luego, en cada iteración, aumentan el nivel de detalle en la estructura del ADN simulada.
Aleksei Aksimentiev y su equipo utilizaron potentes simulaciones computacionales para descubrir cómo los virus empaquetan grandes cantidades de ADN en sus cápsides.
Chris Maffeo/Universidad de Illinois Urbana-Champaign
En su nuevo estudio, los investigadores utilizaron este enfoque para modelar computacionalmente el virus y su ADN durante el ensamblaje viral. Con datos experimentales previos como la estructura de la cápside y la fuerza del motor que carga el ADN en el virus como punto de partida, simularon el comportamiento de cada uno de los 26 millones de átomos durante el caótico proceso de carga del ADN en la cápside. Esta no fue una tarea fácil; cada simulación tardó entre tres meses y un año en ejecutarse, incluso en computadoras muy potentes.
De acuerdo a eric mayo, un biólogo estructural de la Universidad de Connecticut que no participó en este estudio, las simulaciones proporcionaron conocimientos sin precedentes sobre la dinámica entre el genoma, la cápside y otras moléculas del virus que pueden pasar desapercibidas mediante métodos experimentales que sólo pueden obtener la estructura promedio en muchas partículas. “Este enfoque computacional no tiene ese tipo de limitación”, dijo. “Ya conocemos los componentes de las proteínas, pero ahora ver la información genómica con todo detalle atómico es muy emocionante”.
Por ejemplo, los investigadores predijeron que el ADN se empaqueta en la cápside mediante un método llamado extrusión de bucledonde las proteínas fuerzan al ADN a adoptar configuraciones de horquilla.3 Aksimentiev se sorprendió al ver la diversidad de configuraciones genómicas producidas por las simulaciones.
“Intuitivamente pensaríamos que cada configuración podría ser diferente, pero lo que nos sorprendió fue la escala en la que las estructuras eran diferentes”, dijo Aksimentiev. “Si nos fijamos en las partículas virales individuales, se diferencian por la configuración global, que fue introducida por el variado proceso de empaquetado”.
Matías Lobo, biólogo estructural del Instituto de Ciencia y Tecnología de Okinawa que no participó en este estudio, dijo que esto aborda una pregunta de larga data sobre cómo los virus organizan sus genomas. Sin embargo, señaló que el estudio carecía de validación experimental de las estructuras predichas.
Aksimentiev cree que pueden mejorar la simulación para tener en cuenta más fuerzas físicas y depender menos de los datos de entrada experimentales. Su grupo también está ejecutando simulaciones de otros virus que son más complejos. May cree que será fundamental aplicar este modelo a virus patógenos como el VIH y el SARS-CoV-2, aunque son más difíciles de modelar debido a sus genomas de ARN. “Sería interesante de ver [the researchers] intentar avanzar en la dirección de sistemas de gran importancia para la salud pública”, afirmó. “También comprender las etapas de la infección viral: ¿en qué se diferencia la estructura de un virus cuando ingresa a la célula? ¿Cómo se libera el genoma de un virus?
Aksimentiev es optimista en cuanto a que las simulaciones se extenderán a virus más complejos, incluidos los virus de ARN, incorporando datos experimentales más específicos. Su mirada también está puesta en un objetivo aún más elevado: simular una célula entera. “Probablemente no llegue pronto, pero es una especie de Santo Grial”, dijo.
Referencias
1. Coshic K, et al. La estructura y propiedades físicas de una partícula de bacteriófago empaquetada.. Naturaleza. 2024;627(8005):905-914.
2. Maffeo C, Aksimentiev A. MrDNA: un modelo de resolución múltiple para predecir la estructura y dinámica de los sistemas de ADN. Res de ácidos nucleicos. 2020;48(9):5135–5146.
3. Ganji M, et al. Imágenes en tiempo real de la extrusión de bucles de ADN mediante condensina. Ciencia. 2018;360(6384):102-105.