Ramon Sun y su equipo utilizan MALDI-MSI para investigar el metabolismo aberrante en enfermedades como la fibrosis pulmonar.
Cameron Shedlock
La mayoría de las personas dan por sentado la respiración, pero los pacientes con enfermedades pulmonares intersticiales (EPI) recuerdan su importancia cada vez que luchan por respirar. Muchos pacientes con EPI desarrollan fibrosis pulmonar, que es la cicatrización gradual de los pulmones. Este proceso progresivo y fatal resulta de una excesiva la matriz extracelular producción y depósito por fibroblastos y miofibroblastos de pulmón, donde el colágeno, la elastina y los glicanos unidos a N son los componentes principales de la matriz.1 En última instancia, la fibrosis pulmonar provoca el engrosamiento de las paredes alveolares, lo que limita la absorción de oxígeno y provoca dificultad para respirar. EPI con fibrosis pulmonar puede resultar de mutaciones genéticas, una enfermedad subyacente o exposición ambiental a microbios, humo o radiación.2 Si los médicos no pueden encontrar la causa de la fibrosis, diagnostican al paciente con fibrosis pulmonar idiopática (FPI).
Actualmente, sólo existen dos medicamentos antifibróticos avalado por la Administración de Alimentos y Medicamentos para el tratamiento de la fibrosis pulmonar.3 Aunque ambos fármacos retardan la progresión de la enfermedad, ninguno de los tratamientos puede detener o revertir completamente el daño pulmonar, lo que destaca la necesidad de nuevas terapias. Un estudio publicado recientemente en Comunicaciones de la naturaleza sugiere que el glucógeno podría ser un objetivo terapéutico importante.4
Ramón Sol, bioquímico de la Universidad de Florida y autor correspondiente del artículo, estudia las vías metabólicas implicadas en enfermedades como la enfermedad de Alzheimer, el sarcoma de Ewing y el cáncer de pulmón. Cuando la pandemia de covid cerró la investigación no esencial, a Sun se le presentó la oportunidad de estudiar los cambios metabólicos que ocurren durante esta enfermedad infecciosa. “De hecho, obtuvimos algunos pulmones de covid-19 de una persona que terminó falleciendo”, recordó Sun.
Ya no se trata de herramientas que se desarrollan en un laboratorio de ingeniería o de química en algún lugar y que aún esperan ser perfeccionadas. Estos están listos para usar… para la investigación biológica.
Ramón Sun, Universidad de Florida
El metabolismo de los carbohidratos complejos es irregular en muchos trastornos humanos, incluida la neurodegeneración y algunos cánceres, pero los científicos no sabían si era anormal en pacientes con covid. Sun y su equipo de investigación primero escanearon las secciones de tejido pulmonar utilizando imágenes de espectrometría de masas de desorción/ionización láser asistida por matriz (MALDI) (MALDI-MSI), que midieron la abundancia de metabolitos en píxeles individuales. Luego utilizaron una técnica llamada reducción de alta dimensionalidad y agrupamiento espacial (HDR-SC) para clasificar píxeles con niveles de metabolitos similares en grupos. Al comparar las ubicaciones de los grupos con regiones patológicas del pulmón, los investigadores observaron que tres grupos correspondían exactamente a las regiones fibróticas en etapa temprana, media y terminal de los pulmones infectados con SARS-CoV-2, lo que indica que el metabolismo de los carbohidratos complejos es aberrante en estos ámbitos. Para investigar más a fondo esta anomalía, analizaron la abundancia de carbohidratos complejos y descubrieron que los glicanos N-ligados y el glucógeno se acumulaban dentro de las regiones fibróticas de los pulmones.
Dado que los pacientes con FPI tienen fibrosis pulmonar, Sun se preguntó si el metabolismo de los carbohidratos complejos también estaba alterado en esta afección. Utilizando MALDI-MSI, observaron que las áreas ricas en glucógeno y glicanos unidos a N correspondían a regiones fibróticas, lo que indica que esta firma de carbohidratos podría ayudar a los médicos a identificar la fibrosis.
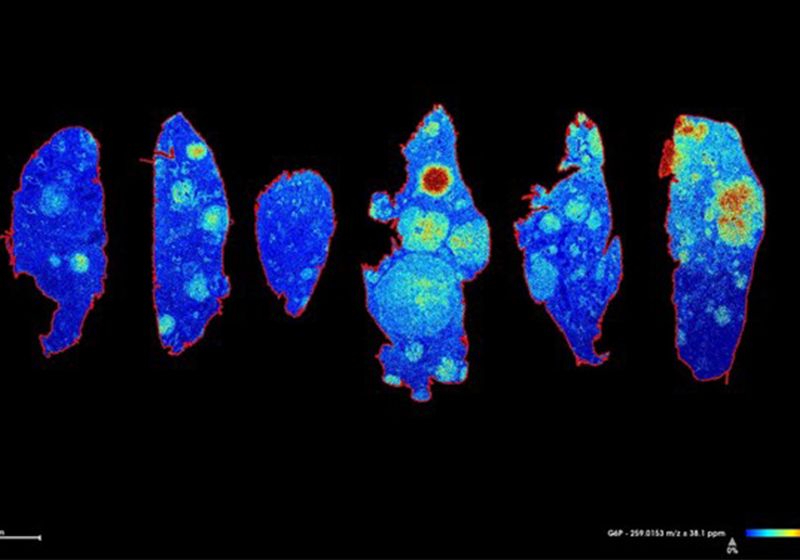
Ramon Sun y sus colegas adquirieron imágenes de espectrometría de masas MALDI como esta, que muestra la abundancia de glucosa 6-fosfato en un modelo de ratón de cáncer de pulmón modificado genéticamente.
Harrison Clark
A continuación, los investigadores cuestionaron si el metabolismo del glucógeno está directamente involucrado en la formación de cicatrices, ya que la descomposición del glucógeno en los lisosomas de miofibroblastos podría proporcionar a las células sustratos para la producción y deposición de glucanos ligados a N. Emplearon modelos de ratón que carecían de las enzimas necesarias para el catabolismo del glucógeno e indujeron lesión pulmonar mediante la administración intratraqueal de bleomicina, un antibiótico utilizado para tratar el cáncer, que provoca una inflamación que luego progresa a fibrosis. A través del análisis MALDI-MSI, los investigadores encontraron menos deposición de glucano ligado a N y fibrosis en los pulmones de ratones incapaces de descomponer el glucógeno, lo que sugirió que la degradación del glucógeno era importante para el desarrollo de la fibrosis pulmonar.
“Creo que la capacidad de localizar señales dentro de un tejido y encontrar estos eventos coordinados en toda la región del tejido y compararlos en una enfermedad, como la fibrosis pulmonar, donde hay tanta heterogeneidad regional, fue muy poderosa”, dijo Nicolás Banovich, un científico genómico del Instituto de Investigación de Genómica Traslacional, que no participó en el estudio. “Quiero ver a estos autores, así como a otros en el campo, continuar desarrollando estos enfoques de espectrometría de masas de imágenes y ver que estas plataformas maduren de la misma manera que estamos comenzando a ver madurar las plataformas transcriptómicas espaciales”.
Sun es optimista en cuanto a que esta investigación podría cambiar la forma en que los médicos tratan y diagnostican la fibrosis pulmonar. Su equipo planea encontrar inhibidores que se dirijan a la síntesis y degradación del glucógeno para convertirlos en terapias para la fibrosis pulmonar. También tiene la intención de crear un protocolo basado en la metabolómica espacial que podría ayudar a los médicos con el diagnóstico de fibrosis pulmonar, ahorrándoles horas al señalar regiones que podrían ser de interés. Además, Sun espera que este artículo inspire a otros investigadores a emplear técnicas de metabolómica espacial en sus laboratorios. “Ya no se trata de herramientas que se desarrollan en un laboratorio de ingeniería o de química en algún lugar y que aún esperan ser perfeccionadas. Están listos para usar… para la investigación biológica”, dijo Sun.
referencias
- Upagupta C, et al. Anomalías de la matriz en la fibrosis pulmonar. Eur RespirRev. 2018;27(148).
- Wijsenbeek M, Cottin V. Espectro de enfermedades pulmonares fibróticas.. N Engl J Med. 2020;383(10):958-968.
- Guo H, et al. Progresos en la comprensión y el tratamiento de la fibrosis pulmonar idiopática: conocimientos recientes y terapias emergentes. Farmacol frontal. 2023;14.
- Conroy LR, et al. La metabolómica espacial revela que el glucógeno es un objetivo viable para la fibrosis pulmonar. comuna nacional. 2023;14(1):2759.